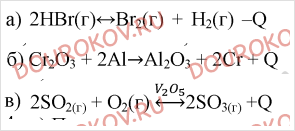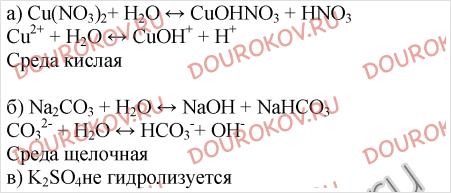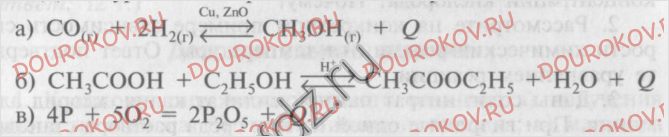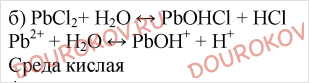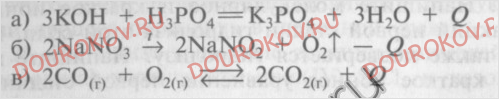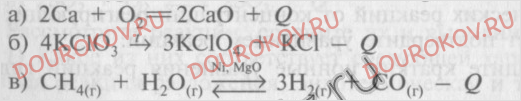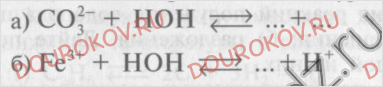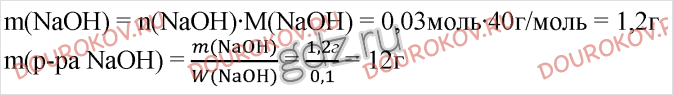Итоговая работа по теме IV
1.Даны уравнения трех химических реакций:
Рассмотрите реакции, сравните их и выполните задания:
1) Какое из них соответствует следующей характеристике: прямая реакция разложения, эндотермическая и т.д.? дополните описание этой реакции.
2) Дайте полную характеристику реакции б.
3) В какую сторону сместится химическое равновесие системы, записанной как уравнение реакции в, при:
а) уменьшении концентрации кислорода; б) повышении температуры; в) понижении давления? Почему?
2. Рассмотрите на конкретном примере зависимость скорости химических реакций от природы реагирующих веществ. Ответ подтвердите уравнением реакции.
3. Даны соли: карбонат натрия, нитрат меди (II), сульфат калия. При гидролизе одной из них среда раствора становится кислой. Напишите молекулярное и краткое ионное уравнения реакций первой стадии гидролиза этой соли. Какая из солей также подвергается гидролизу? Напишите молекулярное и краткое ионное уравнения первой стадии ее гидролиза.
4. К 500 г раствора нитрата свинца прилили избыток раствора сульфида натрия. Масса образовавшегося осадка составила 23,9 г. Рассчитайте массовую дол. Нитрата свинца в исходном растворе.
1. Даны уравнения трех химических реакций:
Рассмотрите реакции, сравните их и выполните задания:
1) Какое из них соответствует следующей характеристике: прямая реакция соединения, экзотермическая и т.д.? дополните описание этой реакции.
2) Дайте полную характеристику реакции б.
3) В какую сторону сместится химическое равновесие системы, записанной как уравнение реакции а: а) при повышении давления; б) при понижении температуры; в) при увеличении концентрации водорода? Почему?
2. Рассмотрите на конкретном примере зависимость скорости химических реакций от концентрации реагирующих веществ. Ответ подтвердите уравнением реакции.
4. Рассчитайте массу соли, которая образовалась при взаимодействии 10 г NaOH и 200 г 15%-ного раствора HBr.
1. Даны уравнения трех химических реакций:
Рассмотрите реакции, сравните их и выполните задания:
1) Какое из них соответствует следующей характеристике: прямая реакция обмена, экзотермическая и т.д.? дополните описание этой реакции.
2) Дайте полную характеристику реакции б.
3) В какую сторону сместится химическое равновесие системы, записанной как уравнение реакции в: а) при повышении температуры; б) при повышении давления; в) при увеличении концентрации кислорода? Почему?
2. Рассмотрите на конкретном примере зависимость скорости химических реакций от температуры. Ответ подтвердите уравнением реакции.
3. Даны соли: нитрат натрия, силикат калия, хлорид алюминия. При гидролизе одной из них среда раствора становится щелочной. Напишите молекулярное и краткое ионное уравнения реакций первой стадии гидролиза этой соли. Какая из солей также подвергается гидролизу? Напишите молекулярное и краткое ионное уравнения реакций первой стадии ее гидролиза.
4. 66,4 мл соляной кислоты (ρ = 1,1 г/мл) полностью прореагировали с 4,48 л аммиака (н.у.). рассчитайте массовую долю HCl в исходном растворе кислоты.
1. Даны уравнения трех химических реакций:
Рассмотрите реакции, сравните их и выполните задания:
1) Какое из них соответствует следующей характеристике: прямая реакция соединения, экзотермическая и т.д.? Дополните описание этой реакции.
2) Дайте полную характеристику реакции б.
3) В какую сторону сместится химическое равновесие системы, записанной как уравнение реакции в: а) при понижении давления; б) при увеличении концентрации метана; в) при понижении температуры? Почему?
2. Рассмотрите на конкретном примере зависимость скорости химических реакций от катализатора. Ответ подтвердите уравнением реакции.
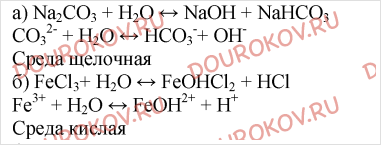
3. Допишите краткие ионные уравнения реакций гидролиза:
Составьте соответствующие им молекулярные уравнения (для первой стадии гидролиза). Какова среда раствора в каждом случае?
4. Для полной нейтрализации порции раствора азотной кислоты ученику потребовалось 1,11 г гидроксида кальция. Какая масса 10%-ного раствора гидроксида натрия необходима ученику для этой же цели взамен гидроксида кальция?
Сохраните или поделитесь с одноклассниками: