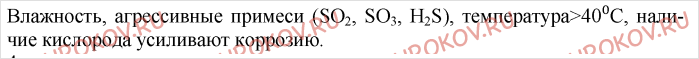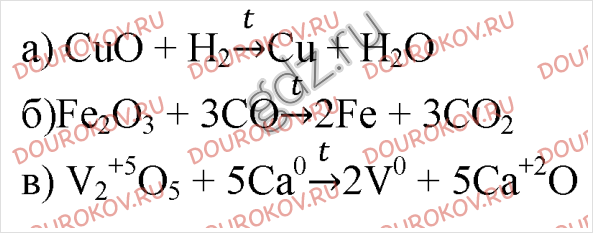Работа 1. Получение металлов. Электролиз. Коррозия металлов
1. Напишите уравнения реакций: а) получения цинка из оксида цинка путем восстановления углём; б) получения кобальта из оксида кобальта (II) путем восстановления водородом; в) получения титана из хлорида титана (IV) магний термическим способом. Реакцию в разберите как окислительно-восстановительную: обозначьте степени окисления атомов и расставьте коэффициенты, определив их методом электронного баланса.
2. Составьте схемы и уравнения реакций, протекающих при электролизе: а) расплава хлорида калия; б) раствора бромида цинка; в) раствора сульфата железа (II).
3. В чем заключается сущность коррозии металлов? Какие виды коррозии вам известны?
Коррозия – это самопроизвольное разрушение металлов и сплавов в результате химического, электрохимического или физико-химического взаимодействия с окружающей средой.
4. На стальной крышке поставлена медная заклёпка. Что раньше разрушится – крышка или заклёпка? Почему?
Стальная крышка, поскольку она включает в себя железо, а железо более активный металл, чем медь и будет скорее коррозировать. Также железо с медью образуют гальваническую пару, где железо – анод, и разрушается скорее, в медь – катод, остается нетронутым.
1. Напишите уравнения реакций: а) получения железа из оксида железа (III) алюминотермическим способом; б) получения меди из оксида меди (II) путём восстановления углём; в) получения вольфрама из его высшего оксида путем восстановления водородом. Реакцию в разберите как окислительно-восстановительную: обозначьте степени окисления атомов и расставьте коэффициенты, определив их методом электронного баланса.
2. Составьте схемы и уравнения реакций, протекающих при электролизе: а) раствора бромида меди (II); б) раствора иодида натрия; в) раствора нитрата свинца (II).
4. Почему лужённый (покрытый оловом) железный бак на месте повреждения защитного слоя быстро разрушается?
Также железо с оловом образуют гальванический элемент, где железо – анод, и разрушается скорее, а олово – катод, остается нетронутым.
1. Напишите уравнения реакций: а)получения меди из оксида меди (II) путём восстановления водородом; б) получения железа из оксида железа (III) путем восстановления оксидом углерода (II); в) получения ванадия из оксида ванадия (V) кальцийтермическим способом. Реакцию в разберите как окислительно-восстановительную: обозначьте степени окисления атомов и расставьте коэффициенты, определив их методом электронного баланса.
2. Составьте схемы и уравнения реакций, протекающих при электролизе: а) расплава хлорида кальция; б) раствора бромида калия; в) раствора сульфата цинка.
3. Какие факторы способствуют замедлению коррозии металлов?
-Нейтрализация или обескислороживание коррозионных сред, а также применение различного рода ингибиторов коррозии;
-Устранения из металла или сплава примесей, ускоряющих коррозионный процесс (устранение железа из магниевых или алюминиевых сплавов, серы из железных сплавов).
-Исключение неблагоприятных металлических контактов или их изоляция, устранение щелей и зазоров в конструкции, устранение зон застоя влаги.
4. Какие металлы при взаимном контакте в присутствии электролита быстрее разрушаются: а) медь и цинк; б) алюминий и железо? Почему?
Быстрее разрушаться будет более активный металл из данной пары
а) цинк более активный металл, чем медь;
б) алюминий более активный металл, чем железо.
1.Напишите уравнения реакций: а) получения молибдена из его высшего оксида путем восстановления водородом; б) получения хрома из оксида хрома (III) алюминотермическим способом; в) получения никеля из оксида никеля (II) путем восстановления углем. Реакцию в разберите как окислительно-восстановительную: обозначьте степени окисления атомов и расставьте коэффициенты, определив их методом электронного баланса.
2. Составьте схемы и уравнения реакций, протекающих при электролизе: а)раствора хлорида меди (II); б) раствора иодида натрия; в) раствора нитрата никеля (II).
4. Почему на оцинкованном баке на месте царапины цинк разрушается, а железо не ржавеет?
Цинк более активный металл, чем железо. Также железо с цинком образуют гальванический элемент, где цинк – анод, и разрушается скорее, а железо – катод, остается нетронутым.
Сохраните или поделитесь с одноклассниками: