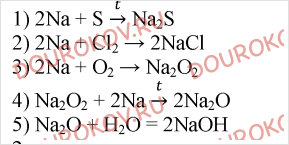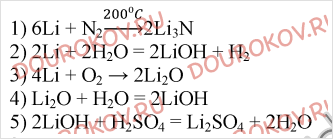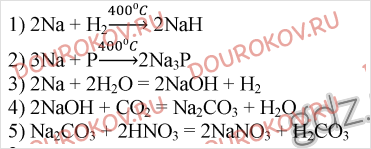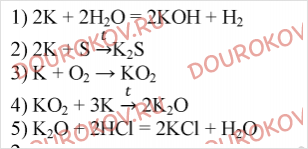Работа 2. Металлы IA-группы
2. Напишите электронные формулы лития, натрия и калия. Сравните строение атомов этим химических элементов, определите черты сходства и различия.
3.При растворении какой массы натрия в воде выделится такой же объем водорода (н.у.), как и при растворении 15,6 г калия?
Щелочные металлы имеют низкие температуры плавления, мягкие, режутся ножом, хорошо проводят электрический ток. На воздухе щелочные металлы мгновенно окисляются. Поэтому их хранят под слоем органических растворителей (керосин, гексан и др.).
3. Для полной нейтрализации 7,3 %-ного раствора соляной кислоты массой 200 г потребовалось 200 г раствора гидроксида натрия. Рассчитайте массовую долю NaOH в этом растворе.
Для всех щелочных металлов характерны восстановительные свойства, т.е. способность атомов легко отдавать свои внешние электроны, превращаясь в положительные ионы. Восстановительная способность увеличивается в ряду –Li–Na–K–Rb–Cs, поскольку увеличивается радиус атома и электрон становится слабее связан с ядром.
3. Рассчитайте массу калия, который прореагировал с водой, если при этом выделилось 4,48 л водорода (н.у.). Рассчитайте массу образовавшегося гидроксида калия.
Щелочные металлы очень химически активны, поэтому встречаются в природе только в виде соединений. Для получения щелочных металлов используют в основном электролиз расплавов их галогенидов, чаще всего – хлоридов, образующих природные минералы. Иногда для получения щелочных металлов проводят электролиз расплавов их гидроксидов.
3. Натрий массой 23 г вступил в реакцию с серой массой 20 г. Рассчитайте массу сульфида натрия, который при этом образовался.
Сохраните или поделитесь с одноклассниками: