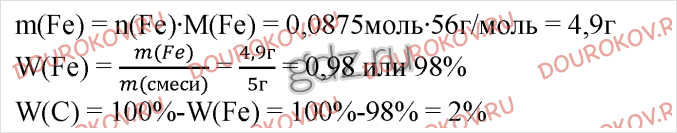Работа 6. Сплавы металлов. Оксиды и гидроксиды металлов
1. Вам выданы склянки с веществами, формулы которых BaO, NaCl, H2O, HNO3, P2O5. Какие реакции, характерные для основным оксидов, можно провести, пользуясь этими веществами? Напишите уравнения всех возможных реакций.
2. Определеите, к какому классу относится вещество, имеющее формулу BeO. Назовите его. Напишите уравнения двух химических реакций, наиболее ярко характеризующих его свойства как представителя указанного вами класса.
3. 30 г сплава меди с цинком обработали раствором серной кислоты. При этом получили 4,4 л водорода (н.у.). Вычислите массовые доли меди и цинка в этом сплаве.
1. Хром образует три оксида: CrO, Cr2O3, CrO3. Укажите, какой из них основный, какой кислотный, а какой амфотерный. Как практически доказать амфотерность оксида?
2. Определите, к какому классу относится вещество, имеющее формулу Ba(OH)2. Назовите его. Напишите уравнения двух химических реакций, наиболее ярко характеризующих его свойства как представителя указанного вами класса.
3. Рассчитайте объем водорода (н.у.), который выделится при действии избытка воды на сплав, содержащий 18,4 г натрия и 15,6 г калия.
1. Оксиды BaO и ZnO представляют собой порошкообразные вещества белого цвета. Если их нельзя различить по внешнему виду, то как это можно сделать при помощи химических реакций? Дайте пояснения и напишите уравнения соответствующих реакций.
2. Определите, к какому классу относится вещество, имеющее формулу Cr2O3. Назовите его. Напишите уравнения двух химических реакций, наиболее ярко характеризующих его свойства как представителя указанного вами класса.
3. При взаимодействии сплава массой 10 г, состоящего из меди и алюминия (бронза), с соляной кислотой выделилось 8 л газа (н.у.). Определите массовую долю каждого металла в сплаве.
1. Как опытным путем определить, является ли выданный вам оксид основным, если он: а) растворим в воде; б) нерастворим в воде? Ответ поясните на конкретных примерах и напишите соответствующие уравнения реакций.
2. Определите, к какому классу относится вещество, имеющее формулу Cr(OH)3. Назовите его. Напишите уравнения двух химических реакций, наиболее ярко характеризующих его свойства как представителя указанного вами класса.
3. Образец сплава железа с углеродом массой 5 г «растворили» в избытке разбавленной серной кислоты. При этом выделилось 1,96 л газа (н.у.). Определите массовую долю каждого компонента сплава.
Сохраните или поделитесь с одноклассниками: