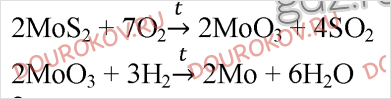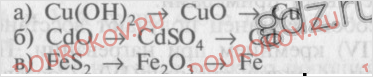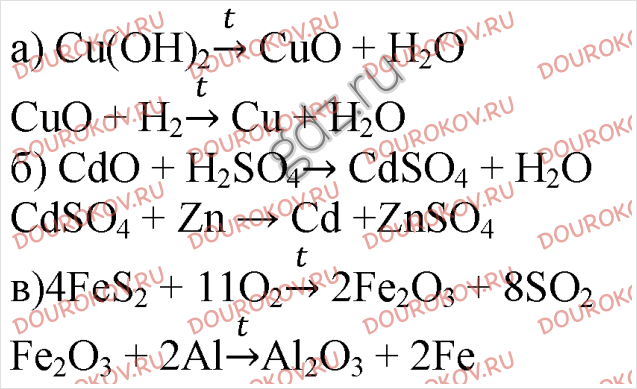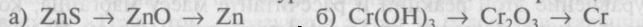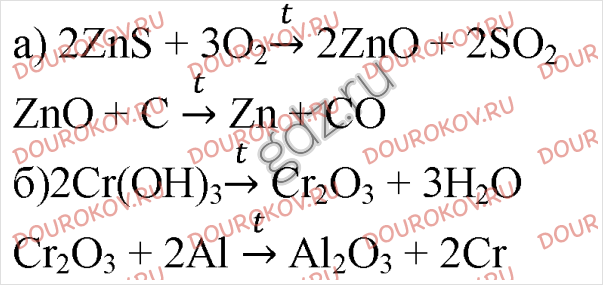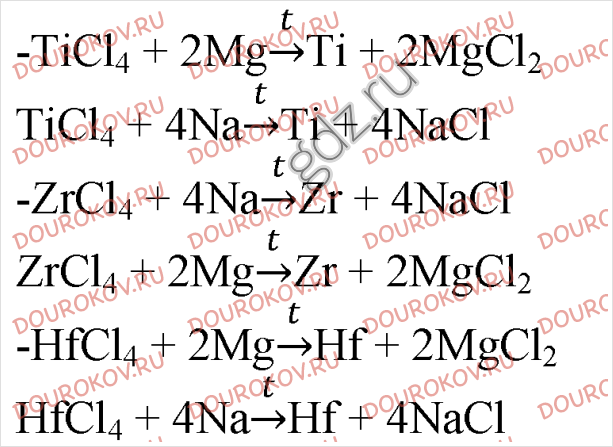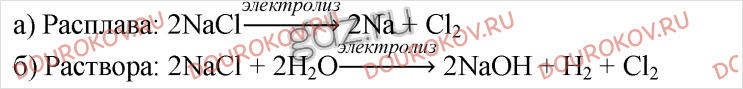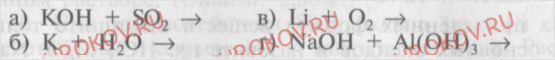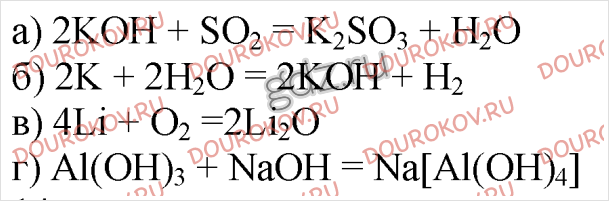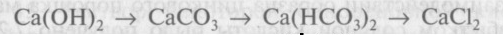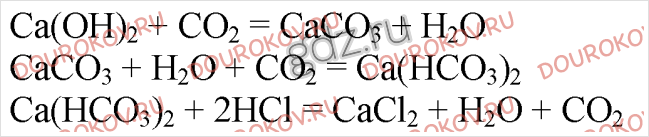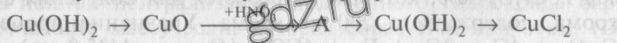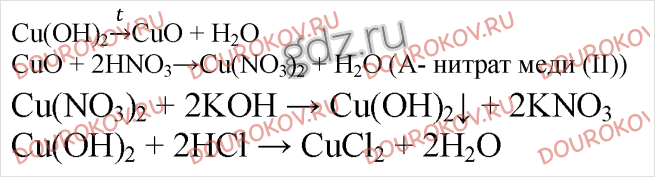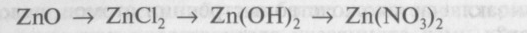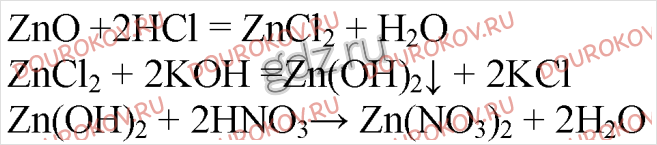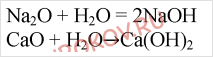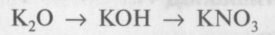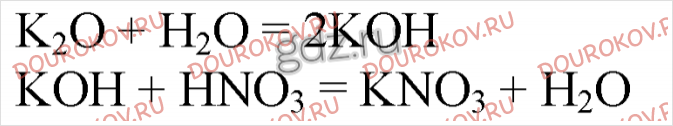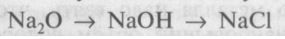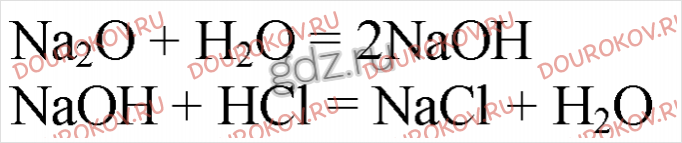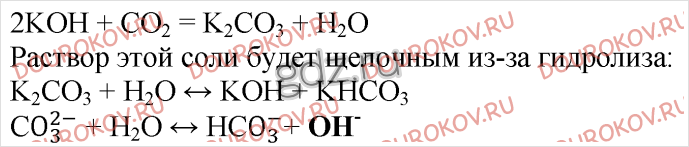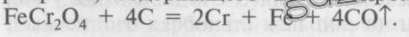Дополнительные задания
1. Молибден получают обжигом минерала молибденита MoS2 с последующим восстановлением оксида молибдена (VI) водородом. Напишите уравнения протекающих реакций.
2. В металлургических процессах восстановление металлов осуществляют сухим способом при высоких температурах (пирометаллургия) или мокрым способом (гидрометаллургия). Приведите примеры получения металлов этими способами.
6. Титан, цирконий и гафний получают восстановлением соответствующих тетрахлоридов магнием или натрием. Составьте уравнения протекающих реакций.
8. Катодом или анодом должно быть металлическое изделие при его хромировании? Дайте обоснованный ответ.
а) электролиз сульфата железа (II) возможен только в растворе, поскольку это соль кислородсодержащей кислоты и на аноде нечему окисляться, нужна вода.
б) электролиз карбоната кальция не возможен, поскольку эта соль не диссоциирует на ионы.
в) электролиз нитрата меди (II) возможен только в растворе, поскольку это соль кислородсодержащей кислоты и на аноде нечему окисляться, нужна вода.
г) сахар – не электролит. Электролиз применим только для электролитов.
10. В чем заключается сходство в строении атомов щелочных металлов?
Щелочные металлы являются s-элементами, т.е. имеют конфигурацию ns1(щелочные металлы) и соответственно один валентный электрон; и ns2 (щелочноземельные металлы) и два валентных электрона. Очевидно, что валентные электроны могут быть легко удалены, потому что атому энергетически выгодно отдать электроны и приобрести конфигурацию инертного газа. Поэтому для всех щелочных и щелочноземельных металлов характерны восстановительные свойства.
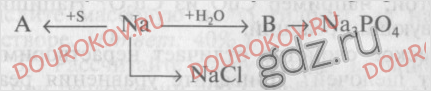
12. Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения:
В одном из окислительно-восстановительных процессов укажите окислитель и восстановитель. Назовите вещества А и В.
Соли получаются в результате нейтрализации (между основанием и кислотой):
NaOH + HCl = NaCl + H2O
15. Гидрид какого щелочного металла надо взять, чтобы получить (в реакции с водой) наибольший объем водорода при одинаковых массах порций гидридов?
16. В раствор сульфата меди (II) поместили кусочек натрия. Напишите уравнения реакций. Которые будут при этом протекать.
Соединения натрия – в желтый
Калия – в фиолетовый
Лития – карминово-красный
Кальция – кирпично-красный
Бария – желтовато-зеленый
18. Почему щелочные металлы встречаются в природе исключительно в виде химических соединений? Напишите формулы известных вам соединений щелочных металлов, встречающихся в природе.
Помимо большей прочности многие сплавы обладают большей коррозионной стойкостью и твердостью, лучшими литейными свойствами, чем чистые металлы. Помимо более высоких механических качеств сплавам присущи свойства, которых нет у чистых металлов. Примерами могут служить получаемая на основе железа нержавеющая сталь – материал с высокой коррозионной стойкостью даже в агрессивных средах и с высокой жаропрочностью; магнитные материалы; сплавы с высоким электрическим сопротивлением, с малым коэффициентом термического расширения. Примеры сплавов: чугун, сталь, бронза, латунь, баббит и др.
21. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Назовите вещество А.
23. Напишите формулы основных оксидов, непосредственно реагирующих с водой. Составьте уравнения протекающих реакций.
Непосредственно с водой реагируют основные оксиды щелочных и щелочноземельных металлов:
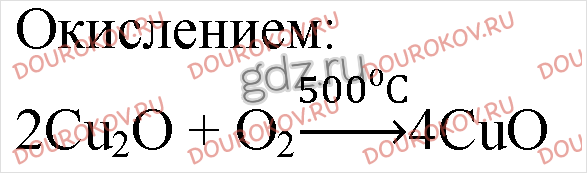
24. Как можно для одного и того же элемента из одного оксида получить другой, например CuO из Cu2O? Напишите уравнения соответствующих реакций.
25. Какое химическое свойство отличает нерастворимые в воде основания от щелочей? Приведите уравнения реакций.
MgO – оксид магния
K2O – оксид калия
CaO – оксид кальция
29. Через раствор гидроксида калия пропустили углекислый газ до полного превращения всей щелочи в карбонат калия. Можно ли утверждать, что полученный раствор соли будет нейтральным? Дайте обоснованный ответ.
30. Определите, к какому классу относится вещество, имеющее формулу KOH. Назовите его. Напишите уравнения двух химических реакций, наиболее ярко характеризующих его свойства как представителя указанного вами класса.
31. Определите, к какому классу относится вещество, имеющее формулу Al2O3. Назовите его. Напишите уравнения двух химических реакций, наиболее ярко характеризующих его свойства как представителя указанного вами класса.
32. При взаимодействии образца цинкового порошка массой 22 г с избытком соляной кислоты было получено 7,2 л водорода (н.у.). вычислите массовые доли цинка и оксида цинка в этом образце цинкового порошка.
33. Рассчитайте массу хромистого железняка с массовой долей FeCr2O4 30%, который потребуется для получения феррохрома, содержащего 200 кг хрома. Уравнение процесса
34. Железная пластинка массой 100 г погружена в раствор сульфата меди (II). Покрывшуюся медью пластинку высушили и снова взвесили. Ее масса оказалась равной 101,3 г. Рассчитайте массу меди, находящейся на пластинке.
35. Стальную проволоку массой 5 г сожгли в кислороде. При этом получили 0,1 г углекислого газа. Вычислите массовую долю углерода в этой стали.
36. Натрий массой 23 г прореагировал с 78 г воды. Вычислите массовую долю гидроксида натрия в полученном растворе.
37. Рассчитайте массу оксида кальция, который образуется при разложении 400 г карбоната кальция, содержащего 6% примесей.
38. Оксид хрома (VI)массой 3 г растворили в 120 г воды. Вычислите массовую долю хромовой кислоты H2Cr2O4 в полученном растворе.
39.При взаимодействии 80 г оксида меди (II) с азотной кислотой был получен 141 г нитрата меди (II). Рассчитайте массовую долю выхода соли.
40. Один из видов бронзы содержит 85% меди, 12% олова и 3% цинка. Рассчитайте объем водорода (н.у.), который выделится при «растворении» 500 г этого сплава в избытке соляной кислоты.
41. 19 г оксида хрома, содержащего 31,58% кислорода, обработали избытком раствора серной кислоты. Рассчитайте массу соли, которая образовалась при этом.
42. 17 г оксида хрома, содержащего 76,47% хрома, обработали избытком соляной кислоты. Рассчитайте массу соли, которая образовалась при этом.
43. 20 г оксида железа, содержащего 70% железа, обработали избытком соляной кислоты. Рассчитайте массу соли, которая образовалась при этом.
44. К 3 г оксида хрома (VI) добавили 120 г воды. Рассчитайте массовую долю хромовой кислоты H2CrO4 в полученном растворе.
45. Раствор некоторой одноосновной кислоты можно нейтрализовать 16 г гидроксида натрия. Рассчитайте массу кристаллогидрата Ba(OH)2 · 8H2O, который необходимо взять для этой цели взамен гидроксида натрия.
46. Оксид бария массой 15,3 г растворили в воде. Рассчитайте объем оксида углерода (IV) (н.у.), который необходим для полной нейтрализации полученного гидроксида бария. Рассчитайте массу соли, которая образуется при этом.
Сохраните или поделитесь с одноклассниками: