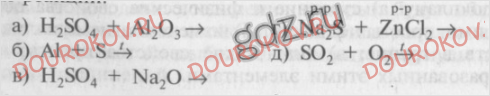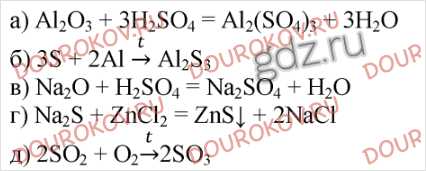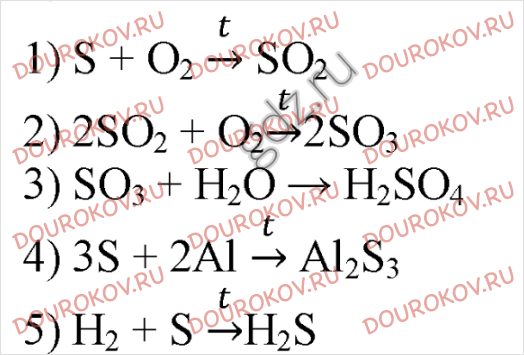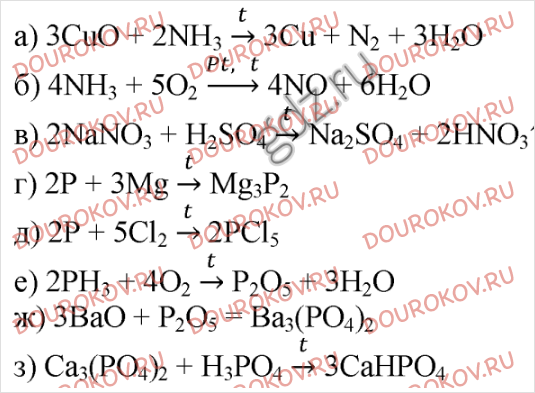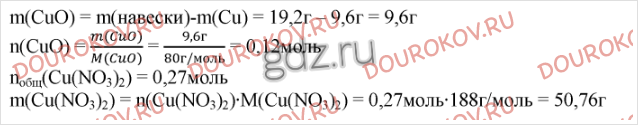Дополнительные задания
3. Чем различаются по составу и свойствам озон и кислород?
Кислород – двухатомная молекула (О₂) бесцветен, не имеет запаха; озон – трехатомная молекула (О₃) имеет выраженный запах, имеет бледно-фиолетовый цвет, обладает бактерицидными свойствами и более реакционноспособный, чем двухатомный кислород.
5. Почему на сернокислотном заводе оксид серы (VI) поглощают не водой, а концентрированной серной кислотой?
7. Рассчитайте, где больше массовая доля серы: а) в хлориде серы S₂Cl₂, используемом в резиновой промышленности как растворитель серы; б) в сульфиде натрия, используемом при производстве серных красителей.
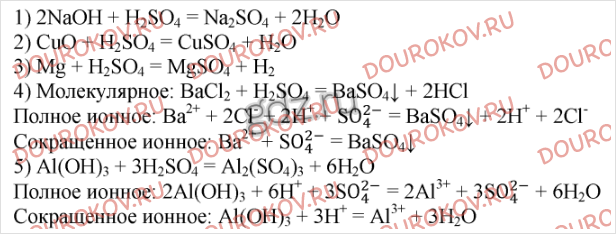
8. С какими из приведенных веществ будет реагировать раствор серной кислоты: гидроксид натрия, оксид меди (II), золото, магний, хлорид бария, серебро, гидроксид алюминия? Напишите уравнения осуществимых реакций (два из них в ионной форме).
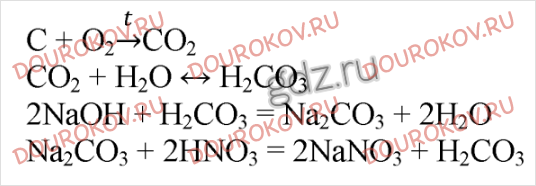
9. Напишите уравнения реакций: а) оксида углерода (IV) с известковой водой; б) оксида углерода (IV) с водой; в) горения угля в избытке кислорода (обозначьте степени окисления атомов, укажите переход электронов, а также окислитель и восстановитель); г) горения оксида углерода (II) в кислороде.
10. Напишите уравнения реакций: а) получения оксида углерода (IV) из известняка промышленным способом; б) углерода с оксидом меди (II); в) углерода с водородом (обозначьте степени окисления атомов, укажите переход электронов, а также окислитель и восстановитель); г) оксида углерода (II) с оксидом свинца (II).
11. Дайте определения адсорбации и десорбации. Укажите, какие области применения древесного угля основаны на его адсорбационной способности.
12. Напишите уравнения реакций: а) оксида углерода (IV) с гидроксидом натрия; б) получения оксида углерода (IV) из мрамора лабораторным способом; в) углерода с серой (обозначьте степени окисления атомов, укажите переход электронов, а также окислитель и восстановитель); г) оксида углерода (II) с оксидом меди (II).
14. В пронумерованных пробирках выданы растворы солей: хлорида калия, карбоната калия, фосфата калия. Как опытным путем их можно распознать? Напишите уравнения соответствующих реакций.
16. Какие изменения наблюдаются при длительном пропускании углекислого газа через известковую воду? Напишите уравнения соответствующих реакций.
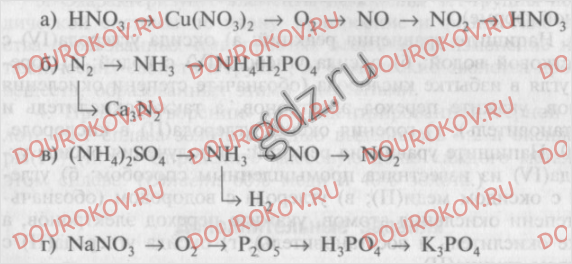
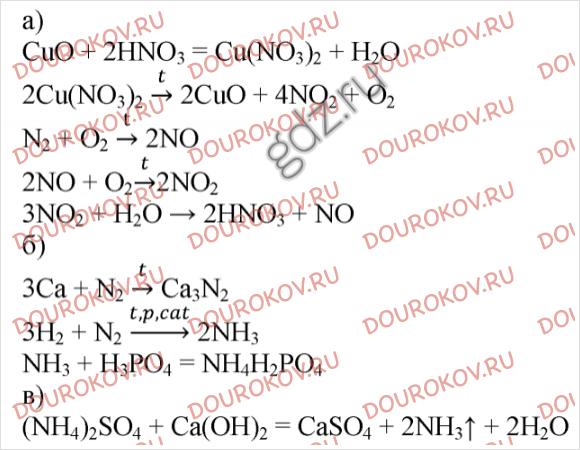
18. Напишите уравнения реакций разложения: а) нитрата калия; б) нитрата меди (II); в) нитрата железа (III). Рассмотрите их как окислительно-восстановительные реакции.
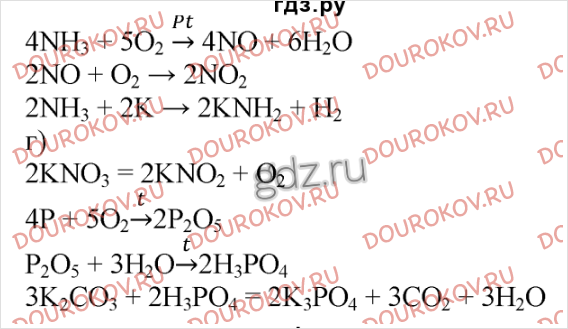
21. Напишите уравнения реакций: а) азота с алюминием (обозначьте степени окисления элементов и укажите окислитель и восстановитель); б) аммиака с бромистым водородом; в) нитрата аммония с гидроксидом кальция при нагревании; г) раствора йодида аммония с раствором нитрата свинца (в молекулярной и ионной формах).
22. Напишите уравнения реакций концентрированной азотной кислоты: а) с серебром; б) со свинцом. Укажите степени окисления элементов и расставьте коэффициенты, определив их методом электронного баланса.
23. Напишите уравнения реакций разбавленной азотной кислоты: а) с цинком; б) с серебром; в) с карбонатом магния; г) с гидроксидом меди (II); д) с оксидом железа (III). Уравнения реакций а и б рассмотрите как окислительно-восстановительные.
25. В трех пронумерованных пробирках выданы растворы фосфорной кислоты, фосфата натрия и соляной кислоты. Как опытным путем их можно распознать? Напишите соответствующие уравнения реакций.
26. Напишите уравнения реакций: а) азота с литием (обозначьте степени окисления атомов и укажите окислитель и восстановитель); б) получения аммиака из соли аммония; в) раствора хлорида аммония с раствором нитрата серебра (в молекулярной и ионной формах).
27. Газовая смесь для синтеза хлороводорода объемом 1 л была пропущена через раствор йодида калия. При этом выделилось 5,08 г йода. Определите объемную долю каждого газа в исходной смеси. (Ответ: 44,8 % хлора и 55,2 % водорода).
28. При анализе природного образца каменной соли в нем обнаружили 55% хлора. Определите массовую долю NaCl в этом образце, если известно, что в нем других соединений хлора не содержится. (Ответ: 90,63%).
29. При взаимодействии 16 г раствора серной кислоты с избытком раствора хлорида бария образовалось 5,7 г осадка. Рассчитайте массовую долю H₂SO₄ в исходном растворе. (Ответ: 15%).
30. Смесь кремния и углерода массой 20 г обработали избытком концентрированного раствора гидроксида натрия. В результате реакции выделилось 13,44 л водорода (н.у.). Определите массовую долю каждого компонента в исходной смеси. (Ответ: 42 % кремния и 58% углерода).
31. Рассчитайте массу нитрата натрия, при разложении которого образуется кислород, объема которого достаточно для полного сжигания: а) 6,2 г фосфора; б) 36 г угля; в) 27,2 г аммиака. (Ответ: а) 42,5 г; б) 510 г; в) 340 г.)
32. Рассчитайте массу силана SiH₄, который образуется при взаимодействии соляной кислоты с 160 г силицида магия Ma₂Si, содержащего 5% примесей. (Ответ: 64 г.)
33. Рассчитайте массу силиката натрия, который образуется при сплавлении 50 г оксида кремния (IV), содержащего 10% примесей, с гидроксидом натрия. (Ответ: 91,5 г).
34. Через раствор, содержащий 1,48 г гидроксида кальция, пропустили 0,336 л углекислого газа. Рассчитайте массу образовавшегося осадка. (Ответ: 1,5 г.)
35. Для получения силиката натрия сплавили смесь, состоящую из 16 г гидроксила натрия и 18 г оксида кремния (IV). Рассчитайте массу соли, которая образовалась при этом. (Ответ: 24,4 г).
36. Газ, полученный при разложении гидрида натрия водой, пропустили над раскаленным оксидом меди (II). При этом масса оксида уменьшилась на 4 г. Рассчитайте массу вступившего в реакцию гидрида натрия. (Ответ: 6 г).
37. 6,72 г смеси газов CO₂ и CO пропустили над раскаленным углем, в результате объем газовой смеси увеличился на 2,24 л. Определите объемную долю каждого газа в исходной смеси. (Ответ: 33,3% CO₂ и 66,7% CO.)
38. Для хлорирования 12 г смеси железа с медью потребовалось 5,6 л хлора (н.у.). определите массовую долю каждого металла в смеси. (Ответ: 46,7% Fe и 53,3% Cu).
39. Навеску смеси меди с оксидом меди (II) с массовой долей меди 50% обработали 30%-ной азотной кислотой. При этом выделилось 2,24 л оксида азота (II) (н.у.). Рассчитайте: а) массу навески; б) массу образовавшейся соли. (Ответ: а) 19,2 г; б) 50,8 г.)
Сохраните или поделитесь с одноклассниками: