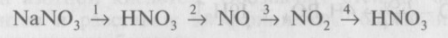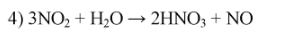Итоговая работа по теме VI
1. Напишите формулы соединений с водородом следующих химических элементов: Na , F, P, O, Cl, Si. Выберите формулы соединений, обладающих кислотными свойствами, и расположите их в порядке усиления кислотных свойств.
Укажите формулу гидрида металла и напишите уравнение реакции его с водой. Определите, как при этой реакции изменяется степень окисления водорода в гидриде металла – повышается или понижается.
2. Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения:
Одну из реакций рассмотрите как окислительно-восстановительную: обозначьте степени окисления элементов и укажите окислитель и восстановитель. Дайте характеристику этой реакции с точки зрения различных классификаций (см. схему в работе 1, тема IV).
3. Охарактеризуйте элементы неметаллы IVA-группы периодической системы химических элементов по плану: а) строение и физические свойства образованных ими простых веществ; б) изменение неметаллических свойств в группе; в) химические свойства простых веществ, образованных этими элементами.
4. Весь хлороводород, полученный действием избытка серной кислоты на хлорид калия массой 14,9 г , взаимодействует с водой массой 200 г. Определите массовую долю хлороводорода в полученном растворе.(Ответ: 3,52%).
1. Напишите формулы водородных соединений всех химических элементов 2-го периода. Выберите из них: а) наиболее типичный гидрид металла; б) самую сильную кислоту.
Найдите в периодической системе такие химические элементы, водородные соединения которых будут обладать еще более выраженными свойствами гидрида металла и кислоты, чем те, которые вы выбрали. Напишите формулы этих водородных соединений.
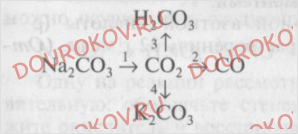
2. Напишите уравнений реакций, при помощи которых можно осуществить следующие превращения:
Выберите окислительно-восстановительную реакцию, обозначьте степени окисления элементов и укажите окислитель и восстановитель. Дайте характеристику этой реакции с точки зрения различных классификаций (см. схему в работе 1, тема IV).
3. Охарактеризуйте элементы VIIA-группы периодической системы по плану: а) строение и физические свойства образованных ими простых веществ; б) изменение неметаллических свойств в группе; в) химические свойства простых веществ, образованных этими элементами.
4. Рассчитайте объем 80%-ной азотной кислоты (p=1.46 г/мл), необходимой для «растворения» 32 г меди . (Ответ: 107,9 мл).
1. Напишите формулы соединений с водородом следующих химических элементов: C, S, N, Br, Cl, Ca. Выберите формулы соединений, обладающих кислотными свойствами, и расположите их в порядке ослабления кислотных свойств. Укажите формулу гидрида металла и напишите уравнение реакции его с водой. Определите восстановитель.
2. Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения:
Выберите окислительно-восстановительную реакцию, обозначьте степени окисления элементов и укажите окислитель и восстановитель. Дайте характеристику этой реакции с точки зрения различных классификаций (см. схему в работе 1, тема IV).
3. Охарактеризуйте элементы VIA-группы периодической системы по плану: а) строение и физические свойства образованных ими простых веществ; б) изменение неметаллических свойства в группе; в) химические свойства простых веществ, образованных этими элементами.
4. Рассчитайте массу меди, прореагировавшей с избытком концентрированной азотной кислоты, если в результате реакции получили 4 л оксида азота (IV) (н.у.). Объемная доля выхода оксида азота (IV) составила 96%. (Ответ: 5,9 г).
1. Напишите формулы водородных соединений всех химических элементов 3-го периода. Выберите из них: а) наиболее типичный гидрид металла; б) самую сильную кислоту.
Найдите в периодической системе такие химические элементы, водородные соединения которых будут обладать еще более выраженными свойствами гидрида металла и кислоты, чем те, которые вы выбрали. Напишите формулы этих водородных соединений.
2. Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения:
Выберите окислительно-восстановительную реакцию, обозначьте степень окисления элементов и укажите окислитель и восстановитель. Дайте характеристику этой реакции с точки зрения различных классификаций (см. схему в работе 1, тема IV).
3. Охарактеризуйте элементы-неметаллы VA-группы периодической системы по плану: а) строение и физические свойства образованных ими простых веществ; б) изменение неметаллических свойств в группе; в) химические свойства простых веществ, образованных этими элементами.
4. При «растворении» в концентрированной серной кислоте 20 г сплава золота с медью выделилось 4,2 л оксида серы (IV) (н.у.). Определите массовую долю каждого металла в этом сплаве. (Ответ: 60% меди и 40% золота).
Сохраните или поделитесь с одноклассниками: