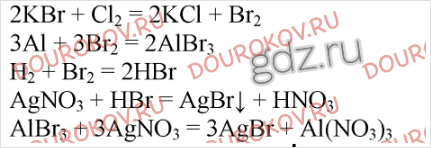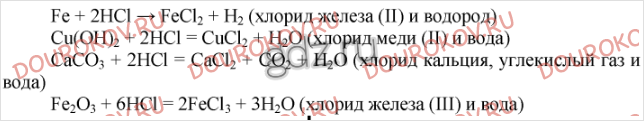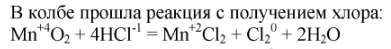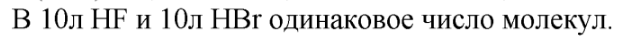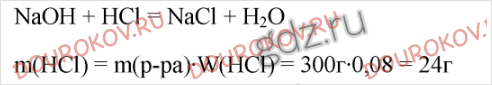Дополнительные задания
1. Даны вещества, формулы которых NaCl, Mg, H₂O, P, KF и CaBr₂. С какими из них будет взаимодействовать хлор? Составьте уравнения возможных реакций. Одну из них разберите как окислительно-восстановительную: укажите степени окисления элементов, а также окислитель и восстановитель.
2. Хлорид железа (III) можно получить: а) взаимодействием железа с хлором; б) действием хлора на раствор хлорида железа (II). Напишите уравнения этих реакций и укажите окислитель.
4. С какими из перечисленных веществ будет реагировать соляная кислота: железо, гидроксид меди (II), золото, карбонат кальция, оксид железа (III)? Напишите уравнения возможных реакций и назовите полученные вещества.
5. Даны растворы веществ, формулы которых BaCl₂, HCl, NaI и KOH. Опишите, как можно распознать эти вещества. Запишите уравнения используемых реакций.
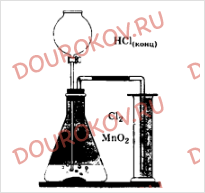
6. Можно ли использовать один и тот же прибор для получения в лаборатории хлора и хлороводорода? Нарисуйте прибор и дайте обоснованный ответ.
7. Напишите известные вам уравнения реакций получения хлорида цинка. В окислительно-восстановительных реакциях укажите окислитель и восстановитель.
8. На весах уравновесили два стакана с соляной кислотой. В один из них поместили кусочек цинка, а в другой – кусочек магния такой же массы. В каком положении будут чашки весов после окончания реакций? Дайте обоснованный ответ и составьте уравнения реакций.
9. Как, имея в своем распоряжении йодид калия, соляную кислоту и оксид марганца (IV), получить йод? Составьте уравнения протекающих реакций и укажите, являются ли они окислительно-восстановительными.
10. Как химическим путем отличить бромид калия от йодида калия? Приведите все известные вам способы распознавания. Напишите уравнения реакций.
11. В колбе нагрели смесь оксида марганца (IV) с концентрированной соляной кислотой. К горлу колбы поднесли влажную йодкрахмальную бумагу (бумага, предварительно пропитанная йодидом калия и крахмалом) – она посинела. Объясните это явление и составьте уравнение реакции.
12. Одинаково ли число молеул: а) в 100 г фтороводорода и 100 г бромоводорода; б) в 10 л фтороводорода и 10 л бромоводорода? Дайте обоснованный ответ.
13. Какой объем бромоводорода (н.у.) потребуется для нейтрализации раствора, содержащего 28 г гидроксида калия?
14. Алюминий массой 5,4 г прореагировал с соляной кислотой. Вычислите: а) объем выделившегося водорода (н.у.); б) массу образовавшейся соли.
15. Через склянку с раствором йодида калия пропустили 4 л воздуха (н.у.), содержащего хлор. При этом выделилось 5,08 г йода. Какова объемная доля хлора в воздухе?
16. Рассчитайте массу алюминия, который должен вступить в реакцию с соляной кислотой, чтобы образовалось 5 моль хлорида алюминия.
17. К раствору, содержащему 2 г бромида кальция, прилили избыток раствора нитрата серебра. Вычислите массу образовавшегося осадка.
18. Рассчитайте массу хлора, который должен вступить в реакцию с йодидом натрия, чтобы получилось 4 моль йода.
20. Рассчитайте массовую долю хлора: а) в тетрахлориде углерода CCl₄; б) в хлориде железа (II); в) в хлороформе CHCl₃; г) в хлориде алюминия.
21. Рассчитайте массу гидроксида натрия, необходимого для полной нейтрализации 300 г раствора соляной кислоты с массовой долей HCl 8%.
Сохраните или поделитесь с одноклассниками: