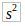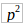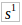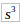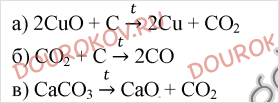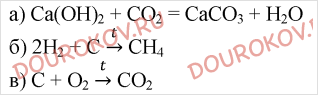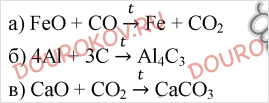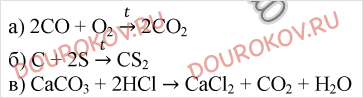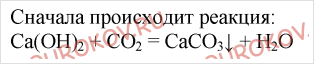Работа 1. Углерод. Оксиды углерода
Вариант 1
1. Изобразите электронную конфигурацию атома углерода в нормальном и возбужденном состояниях. Почему для атома углерода возможен переход электрона по схеме 2
2
→2
→2
?
2. Напишите уравнения реакций: а) углерода с оксидом меди (II); б) углерода с оксидом углерода (IV); в) получения оксида углерода (IV) из известняка промышленным способом.
3. Пропуская водяные пары через раскаленный уголь, получают водяной газ – смесь CO с H₂. Напишите уравнение этой реакции и рассчитайте массу каждого из газов, образующихся при взаимодействии 2,7 кг воды с углем. (Ответ: 4,2 кг CO и 0,3 кг H₂.)
Вариант 2
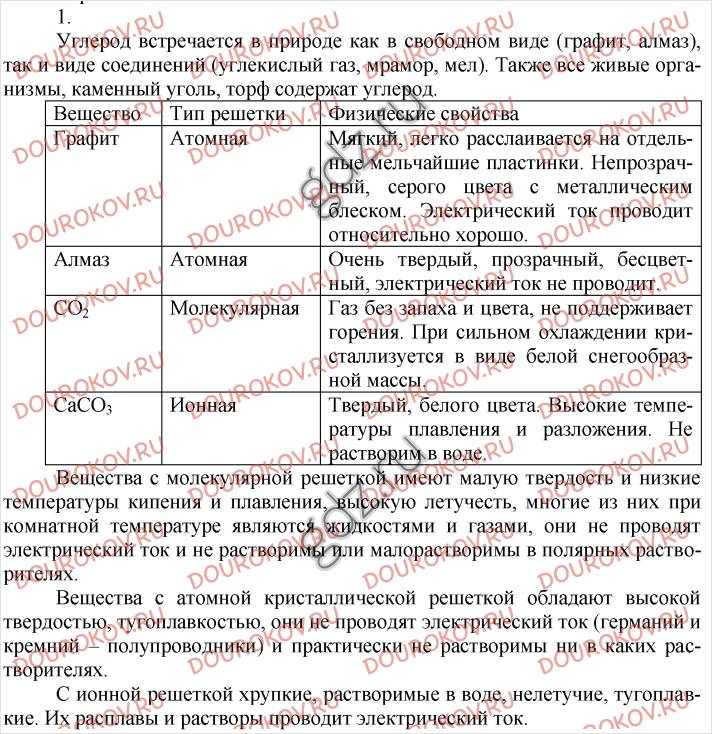
1. В виде каких простых веществ углерод встречается в природе? Сравните их физические свойства. Объясните зависимость физических свойств от структуры кристаллической решетки.
2. Напишите уравнения реакций: а) оксида углерода (IV) с известковой водой; б) углерода с водородом; в) горения углерода в избытке кислорода.
3. Какой объем воздуха (н.у.) расходуется при полном сгорании 84 л оксида углерода (II)? Объемная доля кислорода в воздухе составляет 21%. (Ответ: 200 л.)

Вариант 3
1. Какие степени окисления проявляет углерод в соединениях? Напишите формулы трех соединений, в которых углерод проявляет различную степень окисления.
2. Напишите уравнения реакций: а) оксида углерода (II) с оксидом железа (II); б) углерода с алюминием; в) оксида углерода (IV) с оксидом кальция.
3. Рассчитайте массу 12,6 л смеси, состоящей из оксида углерода (II) и оксида углерода (IV). Объемная доля оксида углерода (IV) в смеси составляет 64 %. (Ответ: 21,51 г.)
Вариант 4
1. Дайте определение адсорбации и десорбации. Укажите, где использую адсорбционную способность древесного угля.
2. Напишите уравнения реакций: а) горения оксида углерода (II); б) взаимодействия углерода с серой; в) получения оксида углерода (IV) из мрамора лабораторным способом.
3. Рассчитайте объемную долю (%) каждого из газов в смеси, состоящей из азота, оксида углерода (II) т оксида углерода (IV), если при пропускании 10 л такой смеси (н.у.) вначале через избыток известковой воды, а затем над нагретым оксидом меди (II) выпадает 15 г осадка и образуется 83,2 г меди. (Ответ: 33,6 % CO₂, 28,7% CO, 37,7% N₂.)
Сохраните или поделитесь с одноклассниками: