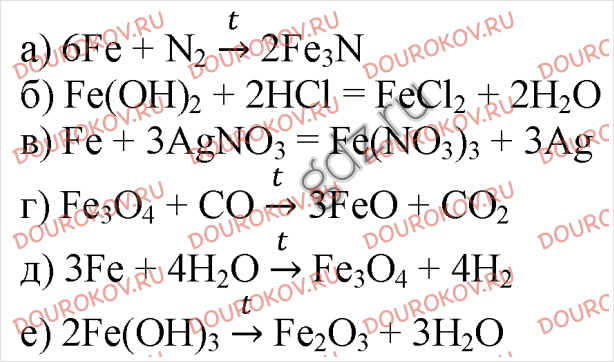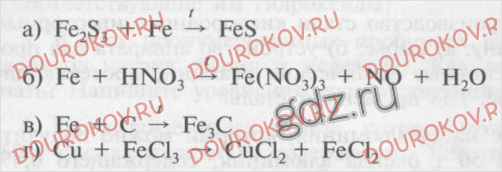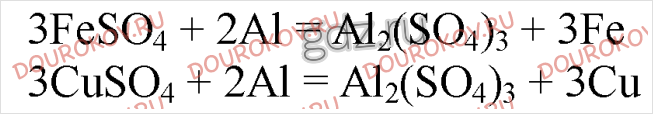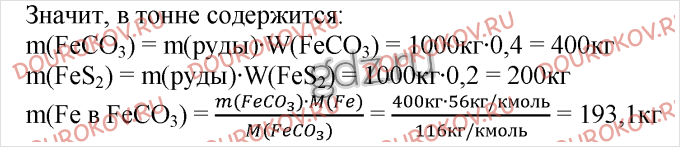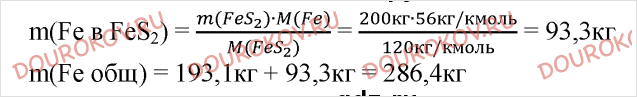Дополнительные задания
1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) Fe→FeCl₂→FeCl₃→Fe(NO₃)₃ →Fe(OH)₃
б) Fe(OH)₃ →FeCl₃→FeCl₂→Fe→Fe₃O₄
3. Даны схемы окислительно-восстановительных реакций:
Обозначьте степени окисления элементов, укажите окислитель и восстановитель. Расставьте коэффициенты, определив их с помощью метода электронного баланса.
4. В смесь растворов сульфата железа (II) и сульфата меди (II) погрузили алюминиевую пластинку. Напишите уравнения протекающих при этом реакций.
5. В каком количестве вещества гидроксида железа (III) содержится столько же железа, сколько в 56 г оксида железа (III)? (Ответ: 0,7 моль).
6. При высокой температуре расплавленное железо реагирует с парами воды с образованием Fe₃O₄ и водорода. Составьте уравнение реакции и рассчитайте массу образовавшегося Fe₃O₄, если было получено 17,92 м3 водорода. Рассчитайте массу железа, которое можно получить из этой массы Fe₃O₄ алюминотермическим методом. (Ответ: 46,4 кг Fe₃O₄ и 33,6 кг Fe).
7. Рассчитайте массу 20%-ного раствора серной кислоты, который необходимо взять для растворения в нем 8,4 г железа. (Ответ: 73,5 г).
8. Рассчитайте объем водорода (н.у.), вступившего в реакцию с оксидом железа (III), если при этом образовалось 252 г железа. (Ответ: 151,2 л).
9. Железная руда содержит 40% сидерита FeCO₃ и 20% пирита FeS₂. Какая масса железа содержится в тонне этой руды? (Ответ: 286,4 кг).
10. Железо, полученное из 24 г оксида железа (III) путем восстановления водородом, сожгли в избытке хлора. Полученную соль растворили в 400 мл воды. Вычислите массовую долю соли (%) в полученном растворе. (Ответ: 10,86%).
11. Рассчитайте объем водорода, который выделится при взаимодействии 2,8 г железа с 20 г 25%-ной соляной кислоты. (Ответ: 1,12 л).
12. Железную пластинку погрузили в раствор сульфата меди. Через некоторое время ее высушили и взвесили. Масса пластинки увеличилась на 2,4 г . Рассчитайте массу железа, перешедшего в раствор. (Ответ: 16,8 г).
13. Сплав железа с углеродом массой 5 г обработали избытком соляной кислоты. По окончании реакции объем выделившегося газа составил 1,96 л (н.у.). Вычислите массовую долю (%) углерода в этом сплаве. (Ответ: 2%).
14. Железную пластинку массой 100 г погрузили в раствор сульфата меди (II). Покрывшуюся медью пластинку высушили и снова взвесили. Ее масса оказалась теперь равной 101,3 г. Какая масса меди осадилась на пластинку? (Ответ: 10,4 г).
Сохраните или поделитесь с одноклассниками: