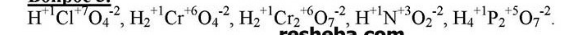§39 Кислоты, их классификация и свойства
- cтраницы 241, 242
1. Выберите формулу сильной кислоты: а) H₂S; б) HNO₃; в) H₂SiO₃. Запишите уравнение диссоциации кислоты.
Сильная азотная кислота:
HNO₃=H++NO₃-
2. Дайте характеристику азотистой кислоты, используя различные признаки классификации кислот.
Азотистая кислота: слабая, одноосновная, кислосодержащая, растворимая в воде, летучая, стабильная.
3. Определите степени окисления элементов в следующих кислотах: хлорной HClO₄, хромовой H₂CrO₄, двухромовой H₂Cr₂O₇, азотистой HNO₂, пирофосфорной H₄P₂O₇.
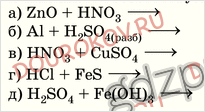
4. Закончите молекулярные уравнения возможных реакций и запишите соответствующие им ионные уравнения:
Если реакция не может быть осуществлена, объясните почему.
5. Рассчитайте объем водорода (н.у.), который выделится при растворении в соляной кислоте 120 г магния, содержащего 2,5% примесей.
6. Запишите формулы оксидов, соответствующих следующим кислотам: HNO₂, HNO₃, H₃PO₄, H₂SO₃, H₂SO₄, H₂SiO₃.
Сохраните или поделитесь с одноклассниками: