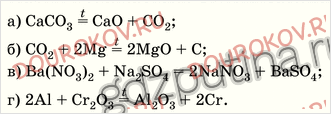§44 Окислительно-восстановительные реакции - cтраницы 268, 269
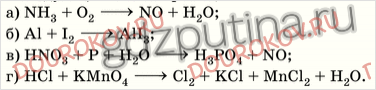
1. Какие из реакций, уравнения которых записаны ниже, относят к окислительно-восстановительным?
Для окислительно-восстановительных реакций укажите окислитель и восстановитель, процессы окисления и восстановления, составьте электронные уравнения.
2. Дайте характеристику реакции синтеза аммиака по всем изученным вами признака классификации химических реакций.
4. Согласны ли вы с утверждением, что HNO₃ проявляет только окислительные свойства, а NH₃ - только восстановительные? Ответ обоснуйте.
5. Какое из веществ – сероводород H₂S и серная кислота H₂SO₄ – проявляет только окислительные или только восстановительные свойства? Почему?
6. Обоснуйте тезис, что SO₂ может быть и окислителем, и восстановителем.
В оксиде SO₂ сера имеет промежуточную степень окисления +4, поэтому в окислительно-восстановительных может проявлять окислительные свойства (принимая электроны и понижая степень окисления до 0 и -2) и восстановительные (отдавая электроны и повышая степень окисления до +6).
8. Назовите окислитель в реакциях взаимодействия цинка с соляной и азотной кислотами. Для последней реакции используйте аналогию взаимодействия азотной кислоты с медью.
Сохраните или поделитесь с одноклассниками: