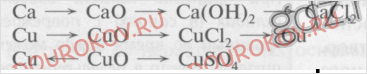
§42 Химические свойства оснований - cтраницы 140, 141, 142, 143, 144, 145, 146
1. Приведите пример реакции нейтрализации. Составьте соответствующее уравнение реакции.
Кислота и щелочь в растворе обмениваются ионами и взаимно нейтрализуют друг друга. Например, NaOH+HCl=NaCl+H₂O.
Гашеную известь широко применяют при строительстве, так как при приготовлении и затвердевании строительного раствора, происходит взаимодействие с углекислым газом из воздуха.
Ca(OH)₂+CO₂=CaCO₃+H₂O
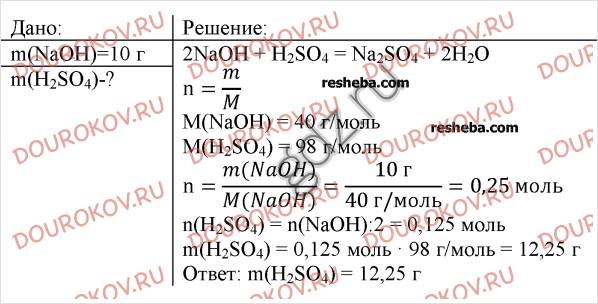
4. Вычислите массу серной кислоты, необходимой для нейтрализации раствора, содержащего 10 г гидроксида натрия.
5. Расположите соединения, формулы которых даны ниже, в порядке возрастания содержания в них железа:
а) Fe₃O₄; б) Fe(OH)₃; в) FeSO₄; г) FeO; д) Fe₂O₃.
ТЕСТОВЫЕ ЗАДАНИЯ
1. Формулы только оснований приведены в ряду
3) KOH, Mg(OH)₂, Cu(OH)₂
2. Индикатор лакмус изменяет свой цвет в щелочной среде
3) на синий
3. Вставьте в схемы реакций нейтрализации недостающие формулы веществ.
1) Mg(OH)₂+HNO₃ → Mg(NO₃)₂+H₂O
2) Mg(OH)₂+HCl → MgCl₂+H₂O
3) KOH+H₃PO₄ → K₃PO₄+H₂O
4) NaOH+H₂S → Na₂S+H₂O
4. Установите соответствие между исходными веществами (веществом) и продуктами химических реакций.
1) –Б, 2) –В, 3) –Г, 4) –А.
NaOH+CO₂ – Na₂CO₃+H₂O
NaOH+H₂SO₄ – Na₂SO₄+H₂O
Fe(OH)₂+HCl – FeCl₂+H₂O
Fe(OH)₂ – FeO+H₂O
Сохраните или поделитесь с одноклассниками: