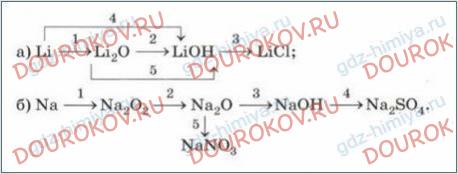
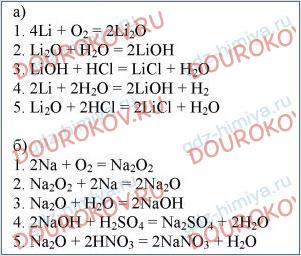
§14. Щелочные металлы - cтраницы 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96
› ГДЗ
2. Вычислите объем водорода (н.у.), который может быть получен при растворении в воде 11,5 г натрия, содержащего 2% примесей, если выход водорода составляет 95% от теоретически возможного.
3. Прочитайте сочинение, написанное ученицей 9 класса 531-й школы Москвы Наташей Фроловой (1991). Какие химические понятия использовала в художественной форме Наташа?
В большом семиэтажном доме, в подъезде щелочных металлов, на втором этаже жил Литий — самый легкий и беззаботный металл. Он, как и все щелочные металлы, очень активно взаимодействовал с кислородом, неметаллами, водородом и водой. Как и все, защищался от кислорода, но носил не керосиновую, а вазелиновую «шубу», так как был очень легким и всплывал в керосине.
Но все же Литий не был во всех отношениях похожим на своих собратьев: он был добр, щедр и прост. Он с охотой отдавал свои электроны и Кислороду, и Азоту, и многим другим элементам. Из-за этих-то особенностей Литий страдал, так как другие щелочные металлы, особенно такие хитрые, как Калий и Натрий, не давали ему прохода. Дело было в том, что, когда щелочные металлы горели в кислороде, каждые их два атома отдавали одной молекуле Кислорода два своих электрона — каждому атому по одному. Остальные электроны они припрятывали до поры до времени. Литий же был честен — отдавал молекуле Кислорода в два раза больше электронов, чем остальные металлы: на четыре атома Лития — четыре электрона. Да и с Азотом Литий взаимодействовал спокойно, при обычной температуре, не то что другие — при нагревании.
И решили Натрий и Калий допытаться у Лития: почему он так поступает? Нет ли в его поведении каких-либо скрытых выгод?
Спрашивает Натрий: «Почему ты, брат Литий, все свои электроны Кислороду отдаешь? Не лучше ли делать так, как мы?» Отвечал Литий: «Я всегда рад помочь другим, не то что вы — жадничаете. Я рад, что в моем оксиде Кислород имеет свою обычную степень окисления -2, не то что -1 в ваших странных, ни на что не похожих пероксидах». Сказал так и ушел восвояси. Долго стояли Натрий и Калий в раздумье, но так ничего и не поняли. И сейчас с Кислородом продолжают пероксиды образовывать. А оксиды состава М2O дают лишь тогда, когда их силой заставят, т. е. создадут соответствующие условия — нагревают пероксид (Na2O2) с таким же металлом — «жадиной (Na)».
Семиэтажный дом— периодическая таблица; подъезд щелочных металлов — I группа элементов; вазелиновая «шуба» способ хранения лития под слоем вазелина. Также Наташа использовала художественный язык для описания и объяснения химических свойств Li (восстановительные свойства, реакция с кислородом).
В большом семиэтажном доме, в подъезде щелочных металлов, на втором этаже жил Литий — самый легкий и беззаботный металл. Он, как и все щелочные металлы, очень активно взаимодействовал с кислородом, неметаллами, водородом и водой. Как и все, защищался от кислорода, но носил не керосиновую, а вазелиновую «шубу», так как был очень легким и всплывал в керосине.
Но все же Литий не был во всех отношениях похожим на своих собратьев: он был добр, щедр и прост. Он с охотой отдавал свои электроны и Кислороду, и Азоту, и многим другим элементам. Из-за этих-то особенностей Литий страдал, так как другие щелочные металлы, особенно такие хитрые, как Калий и Натрий, не давали ему прохода. Дело было в том, что, когда щелочные металлы горели в кислороде, каждые их два атома отдавали одной молекуле Кислорода два своих электрона — каждому атому по одному. Остальные электроны они припрятывали до поры до времени. Литий же был честен — отдавал молекуле Кислорода в два раза больше электронов, чем остальные металлы: на четыре атома Лития — четыре электрона. Да и с Азотом Литий взаимодействовал спокойно, при обычной температуре, не то что другие — при нагревании.
И решили Натрий и Калий допытаться у Лития: почему он так поступает? Нет ли в его поведении каких-либо скрытых выгод?
Спрашивает Натрий: «Почему ты, брат Литий, все свои электроны Кислороду отдаешь? Не лучше ли делать так, как мы?» Отвечал Литий: «Я всегда рад помочь другим, не то что вы — жадничаете. Я рад, что в моем оксиде Кислород имеет свою обычную степень окисления -2, не то что -1 в ваших странных, ни на что не похожих пероксидах». Сказал так и ушел восвояси. Долго стояли Натрий и Калий в раздумье, но так ничего и не поняли. И сейчас с Кислородом продолжают пероксиды образовывать. А оксиды состава М2O дают лишь тогда, когда их силой заставят, т. е. создадут соответствующие условия — нагревают пероксид (Na2O2) с таким же металлом — «жадиной (Na)».
Семиэтажный дом— периодическая таблица; подъезд щелочных металлов — I группа элементов; вазелиновая «шуба» способ хранения лития под слоем вазелина. Также Наташа использовала художественный язык для описания и объяснения химических свойств Li (восстановительные свойства, реакция с кислородом).
4. Напишите сочинение о щелочных металлах, положив в основу сюжета превращения этих металлов или какой-ли-бо один химический процесс.
Предоставляем вам возможность подумать над этим самим. Как тему для сочинения можно взять окраску пламени щелочных металлов.
Предоставляем вам возможность подумать над этим самим. Как тему для сочинения можно взять окраску пламени щелочных металлов.
5. В 100 г кураги содержится 2,034 г калия. Сколько граммов кураги нужно съесть, чтобы получить суточную норму калия?
Сохраните или поделитесь с одноклассниками: